A Anvisa é o órgão regulador do Ministério da Saúde e é responsável por fiscalizar a fabricação e comercialização de produtos para saúde. Essa prática ajuda a garantir a qualidade e a segurança das informações. O registro de produto é uma certificação fornecida pela Anvisa que permite ao fornecedor vender alimentos, medicamentos, produtos afins, saneantes e cosméticos e declarar que está apto para uso.
A Resolução da Comissão Colegiada 185 (RDC) (outubro de 2001) estabelece que “os fabricantes ou importadores de produtos médicos devem apresentar à ANVISA a documentação para registro, alteração, revalidação ou cancelamento de registro”. Na definição de produtos médicos, são descritos como “produtos destinados à saúde, tais como equipamentos, instrumentos, materiais, artigos ou sistemas para uso ou aplicação médica, odontológica ou laboratorial, para fins de prevenção, diagnóstico, tratamento, reabilitação ou anticoncepcional (…)”. Dito isso, sistemas como o PACS também se enquadram nessa categoria e exigem registro adequado.
Entender o processo de registro de um produto médico na ANVISA é muito importante para quem deseja entrar nesse segmento de mercado. São produtos diretamente relacionados ao bem-estar e à vida humana, há muitas exigências para sua comercialização.
Para as instituições médicas, adquirir produtos aprovados pela Anvisa é ter confiança no consumo. Com a certificação, a Anvisa garante que um produto passou por um teste de verificação de qualidade. Dessa forma, os profissionais de saúde têm mais confiança no uso de um determinado produto e, portanto, mais confiança no diagnóstico/tratamento dos pacientes. Também é importante lembrar que as empresas responsáveis pelo desenvolvimento desses produtos podem ser auditadas pela Anvisa a qualquer momento para garantir a conformidade da produção.
ANVISA
Tem como finalidade institucional o controle higiênico da produção e consumo de produtos e serviços com fiscalização higiênica, incluindo o meio ambiente, processos, insumos e tecnologias a eles associados, bem como o controle de portos, aeroportos, fronteiras e instalações alfandegárias.
Produtos de saúde
Um produto de saúde é um dispositivo, instrumento, material, artigo ou sistema para uso ou aplicação médica, odontológica ou laboratorial, destinado à prevenção, diagnóstico, tratamento, reabilitação ou contracepção e sem o uso de meios farmacológicos, imunológicos ou metabólicos para realizar sua função primária. função em humanos, mas pode auxiliar sua função desta forma. Vide Anexo I da Resolução 185 de 22 de outubro de 2001 RDC.
Produtos médicos ativos
Qualquer produto médico cujo funcionamento dependa de uma fonte de energia elétrica ou qualquer outra fonte de energia que não seja a produzida pelo corpo humano ou pela gravidade, e funcione convertendo essa energia.
Produtos médicos ativos para uso diagnóstico
Qualquer produto médico ativo usado sozinho ou em combinação com outros produtos médicos destinados a fornecer informações para a detecção, diagnóstico, monitoramento ou tratamento de uma condição fisiológica ou de saúde, doença ou malformação congênita.
Produtos médicos ativos para uso terapêutico
Qualquer produto médico ativo, usado sozinho ou em combinação com outros produtos médicos, projetado para apoiar, modificar, substituir ou restaurar a função ou estrutura biológica para tratar ou aliviar doenças, lesões ou deficiências.
Ação de campo
Uma ação tomada pelo fabricante ou detentor de registro de um produto para saúde para reduzir o risco de eventos adversos associados ao uso de um produto para saúde comercializado. Exemplos de ações importantes tomadas pela empresa incluem: recalls de produtos, correções de produtos no local, atualizações de software e cartas aos clientes com descrições dos problemas encontrados. É dever das empresas fabricantes e detentoras de registro, estruturar e gerenciar as ações de campo dos produtos registrados no Brasil, conforme descrito na Resolução da Diretoria Colegiada – RDC/Anvisa nº 551/2021.
Em 1 ano aconteceram 198 ações de campo para equipamentos médicos
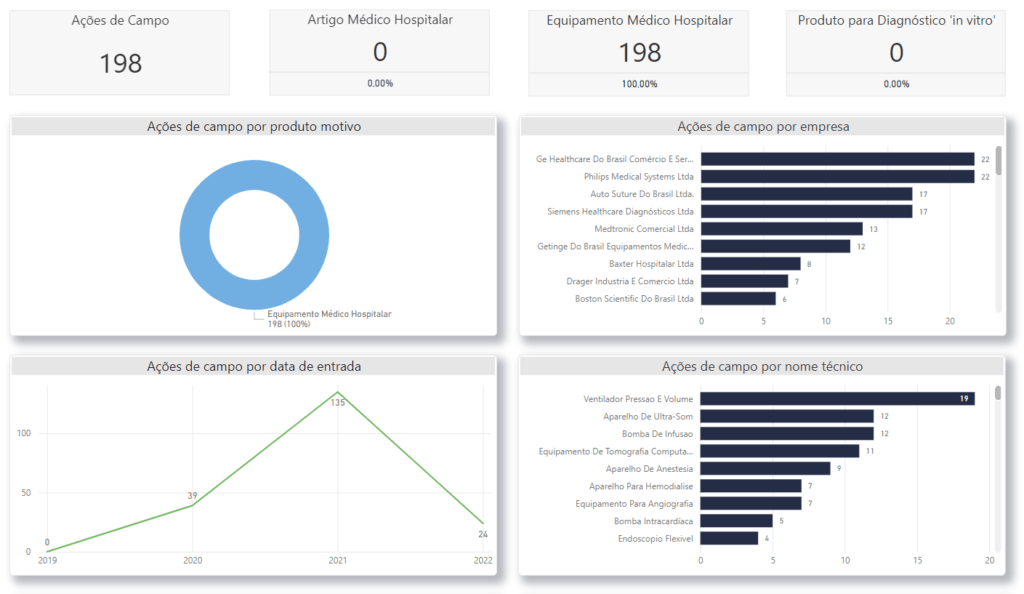
A Tecnovigilância
Inclui um sistema de monitoramento de eventos adversos e reclamações técnicas de produtos de saúde disponíveis no mercado (dispositivos, materiais, insumos médico-hospitalares, implantes, produtos de diagnóstico para uso “in vitro”) para recomendar medidas a serem tomadas para garantir o uso de estes A segurança higiênica dos produtos na promoção e proteção da saúde da população.
